中國浙江華海製藥公司「纈沙坦」(valsartan)原料藥含動物致癌成分的不純物「N-亞硝基二甲胺」(NDMA)事件,風暴再擴大。食藥署今晚宣布,「珠海潤都製藥公司」的同款降血壓藥也出包,台灣4款藥品遭到波及,即日起下架回收。
中國浙江華海製藥公司製造的原料藥,日前傳出含致癌疑慮的不純物。食藥署今晚宣布,「珠海潤都製藥公司」的同款降血壓藥也出包,即日起下架,預計將回收2421萬顆,未出貨部分則禁止出貨。
食藥署指出,問題藥風波起源自7月初,中國大陸浙江華海製藥公司生產的高血壓藥,被發現含疑似致癌物質「N-亞硝基二甲胺」(NDMA),當時調查發現,全台有6款藥品受波及,1000多萬顆藥品下架回收。
依據原料藥業者調查報告及國際藥政管理單位的推論,該不純物產生原因可能與製程相關,推測類似製程的原料藥也可能產生NDMA。食藥署考量我國尚有輸入其他來源的valsartan原料藥,全面進行調查。
結果進一步發現,中國「珠海潤都製藥公司」生產的valsartan原料藥檢出NDMA不純物,而該原料藥使用於我國生達化學製藥股份有限公司4項藥品。該公司經自主送驗原料藥,亦檢出含有NDMA,於8月2日主動進行該等藥品全面回收作業,4項藥品共生產51批,其中已出貨的49批(約2421萬顆)立即回收,未出貨2批禁止出貨。
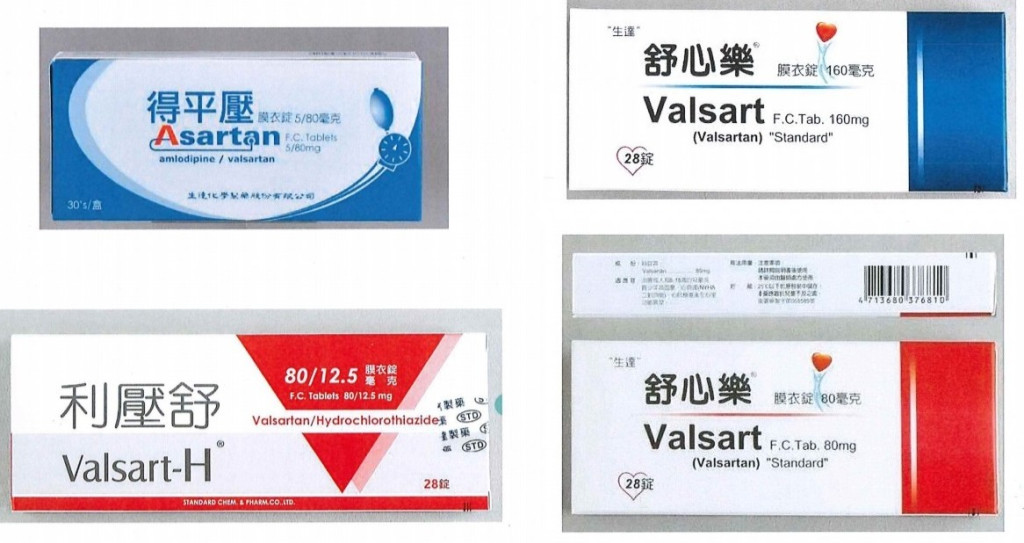
回收藥品明細如下:
一、"生達”舒心樂膜衣錠 160 毫克(衛署藥製字第055557號)。
二、“生達”舒心樂膜衣錠 80 毫克(衛署藥製字第055585號)。
三、得平壓膜衣錠5/80毫克(衛部藥製字第058570號)。
四、利壓舒膜衣錠80/12.5毫克(衛部藥製字第059809號)。
食藥署除請該公司立即通知下游醫療機構及藥局,即刻起下架停止供應,並於1個月內、亦即本(8)月31日完成回收,同時請衛生局督導下架回收事宜,業者於更換其他原料藥前暫停生產販售。
食藥署提醒正在使用該等藥品的病人,該等藥品主要用於高血壓等需定期服藥控制之疾病,不建議任意停藥,應盡速回診時,與醫師討論,處方其他適當藥品。